
Critères d'inclusion
Dès lors qu’ils sont diagnostiqués à partir du 1er janvier 1988 chez des personnes qui résident dans le Haut-Rhin au moment du diagnostic, le Registre inclut dans sa base les cas suivants :
- toutes les tumeurs incidentes selon les critères du Centre international de recherche sur le cancer (CIRC), de l’European Network of Cancer Registries (ENCR) et du réseau Francim :
- les tumeurs malignes invasives (dont les carcinomes épidermoïdes de la peau),
- les tumeurs bénignes ou non invasives de l’appareil urinaire,
- les tumeurs intracrâniennes et intramédullaires quel que soit leur comportement tumoral, à l’exception des adénomes hypophysaires, des lésions vasculaires bénignes des méninges (hémangiomes) et des lésions kystiques (sauf kystes dermoïdes),
- les hémopathies malignes,
- S’ils sont diagnostiqués depuis le 1er janvier 1991, sont également inclus :
- les carcinomes basocellulaires cutanés,
- les tumeurs malignes non infiltrantes, dites in situ ou intraépithéliales, lorsqu’aucune tumeur invasive de même type histologique et de même localisation n’est précédemment apparue chez la même personne,
- les lésions précancéreuses du col de l’utérus,
- les tumeurs à la limite de la malignité (borderline) de l’ovaire,
- les tumeurs stromales gastro-intestinales bénignes et à malignité incertaine (GIST).
Aujourd’hui en France, le Registre des cancers du Haut-Rhin est le seul registre à poursuivre le recensement des carcinomes basocellulaires cutanés (devant leur évolution purement locale qui ne provoque pas de métastase, leur caractère multirécidivant et leur nombre important, les autres registres ont fait le choix de ne pas enregistrer ces cancers dans leurs bases).
Méthodes d'enregistrement
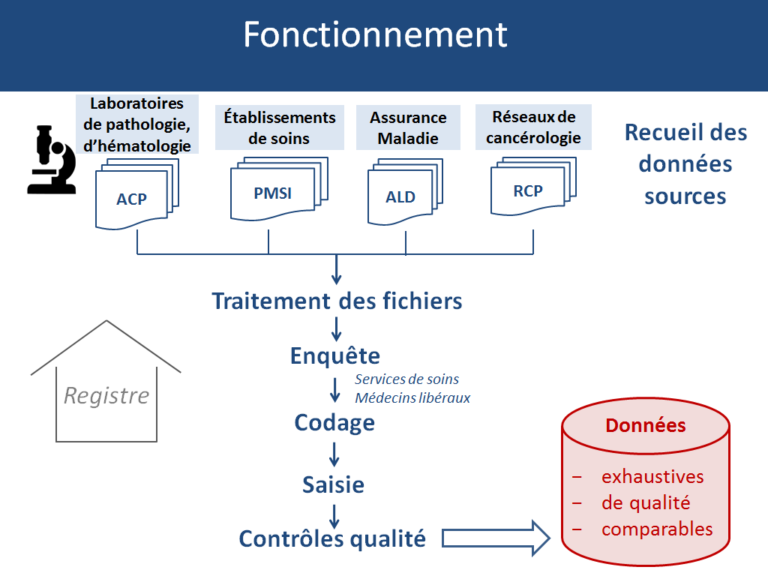
Sources de signalement des cancers
Enquête, codage et saisie
Après croisement et vérification de ces informations « sources », les cas sont enregistrés selon des procédures standardisées internationales (CIRC : Centre international de recherche sur le cancer, ENCR : réseau européen des registres des cancers) et nationales (Francim : réseau français des registres de cancer), permettant d’assurer la comparabilité des données avec les autres registres des cancers.
Les données recueillies sont les suivantes :
- informations sur l’identité et l’adresse du patient, indispensables pour le croisement des informations de sources différentes et l’élimination des doublons,
- informations médicales nécessaires à l’analyse, la validation, la vérification et le suivi des cas,
- sources de signalement et éventuelles sources médicales complémentaires ayant permis de confirmer le cas,
- informations sur les traitements et l’évolution éventuelle de la tumeur.
La localisation et l’histologie de la tumeur primitive sont codées selon la Classification internationale des maladies en oncologie – 3ème édition (CIM-O-3).
Les évolutions de nomenclatures font référence aux mises à jour de l’OMS (WHO Classification of Tumours).
Le stade tumoral est déterminé à l’aide de la classification TNM, à partir des éléments contenus dans les dossiers médicaux (UICC).
Les données sont saisies dans une application spécifiquement dédiée au Registre et pour laquelle toutes les mesures de sécurité physique et logique sont assurées selon les recommandations de la Commission nationale de l’informatique et des libertés (CNIL) et du Règlement général sur la protection des données (RGPD).
Contrôles qualité et validation des données
Les procédures de contrôles de cohérence, de qualité et d’exhaustivité font référence aux règles éditées par le CIRC et l’ENCR pour les registres du cancer, complétées de règles internes spécifiques. Ces contrôles sont régulièrement effectués sur la base de données du Registre.
Des recherches de doublons sont réalisées systématiquement à la saisie et périodiquement sur l’ensemble de la base. Des contrôles de cohérence sont réalisés à la saisie et périodiquement notamment grâce aux logiciels développés par l’ENCR et le CIRC.
L’exhaustivité de l’enregistrement par le Registre est vérifiée à la fin de chaque nouvelle année de diagnostic (pourcentage de vérification microscopique, nombre moyen de sources par cas, ratio mortalité/incidence, évolution de l’incidence par localisation tumorale).
Une fois validées, les données peuvent être utilisées pour la veille sanitaire ou la recherche après anonymisation. Les données anonymisées sont également transmises à la base commune des registres.
